日前,美国食物药品治理局药物评价及研究中央(CDER)发布2022年度新药获批陈诉。按照陈诉,2022年,美国食物药品治理局(FDA)共核准了37款新药,包括22款新份子实体及15款生物成品。此外,还有有2款疫苗、5款细胞与基因疗法,以和1款微生物组疗法。
与往年比拟,2022年FDA核准的新药数目有所降落,但立异程度依然很高。获批的生物成品类型富厚,笼罩单抗、双抗、抗体偶联药物(ADC)、T细胞受体(TCR)疗法等。以疾病范畴划分,2022年FDA核准的新药(不包括疫苗、基因疗法及细胞疗法)中肿瘤药占比最高,其次是神经体系类药物。
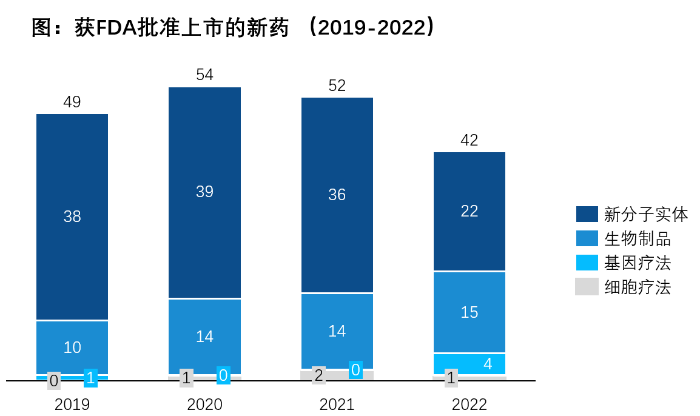
图 2019-2022年获美国FDA核准上市的新药
来历:美国FDA(截至2022.12.31),沙利文阐发
FDA经由过程快速通道认定、优先审评认定、冲破性医治认定以和加快核准等四种通道加速新药研发与审评。于2022年获批的新药中,有12款新药得到快速通道资历,21款新药经由过程优先审评的方式上市,13款产物被FDA授予了冲破性疗法的资历认定,还有有6款经由过程加快核准步伐上市。从药物立异性来看,有20款立异药具备全新的、怪异的作用机制,被认定为“First-In-Class”疗法,占整年获批新药总数的54%。
2022年,我国本土企业南京传奇“出海”乐成,与美国强生互助的CAR-T产物——西达基奥伦赛,为整年独一一款得到FDA核准上市的细胞疗法产物。此外,于4款获批的基因疗法中,稀有病范畴体现亮眼,共有3款稀有病药物问世:
2022年8月17日,FDA核准蓝鸟生物(Bluebird Bio)的基因疗法Zynteglo(betibeglogeneautotemcel,beti-cel),用在医治β地中海血虚。
2022年9月16日,FDA正式核准蓝鸟生物的基因疗法SKYSONA(elivaldogeneautotemcel,Lenti-D™)上市,用在医治春秋于4到17岁、携带ABCD1基因突变、初期脑型肾上腺脑白质养分不良(CALD)的男性患者。
2022年11月23日,FDA核准了CSL Behring公司的Hemgenix(etranacogenedezaparvovec),用在医治今朝利用因子IX预防疗法或者今朝有血友病B(天赋性因子IX缺少症)的成人或者既往有危和生命的出血史,或者有重复、严峻的自觉性出血事务。
(作者单元:弗若斯特沙利文)

AI怎样向羁系证实本身?
进一步将羁系要求落地为可操作的可托度证实路径。FDA指出,该指南草案面向利用AI天生信息或者数据,用在撑持药品与生物成品安全性、有用性和质量相干的羁系决议计划,不涵盖仅用在药物发明或者纯真晋升... 2026-04-16 08:58
2月份美国Clinicaltrial数据库临床实验数据显示—— 糖尿病、乳腺癌、肥胖等顺应证成研发烧点
按照美国Clinicaltrial数据库数据,本年2月份,全世界新开由企业本钱主导的临床实验总数为707项,数目较1月份降落5.23%;单月新开临床实验数目高在去年同期程度,同比上升16.67%。热点范畴漫衍从2... 2026-04-09 13:33-米兰·(milan)




























 粤公网安备 44011202003184号
粤公网安备 44011202003184号